Covid-19| Cât de mult vor risca primii pacienți care se vor vaccina. „O atenție specială efectelor secundare pe termen mediu și lung”
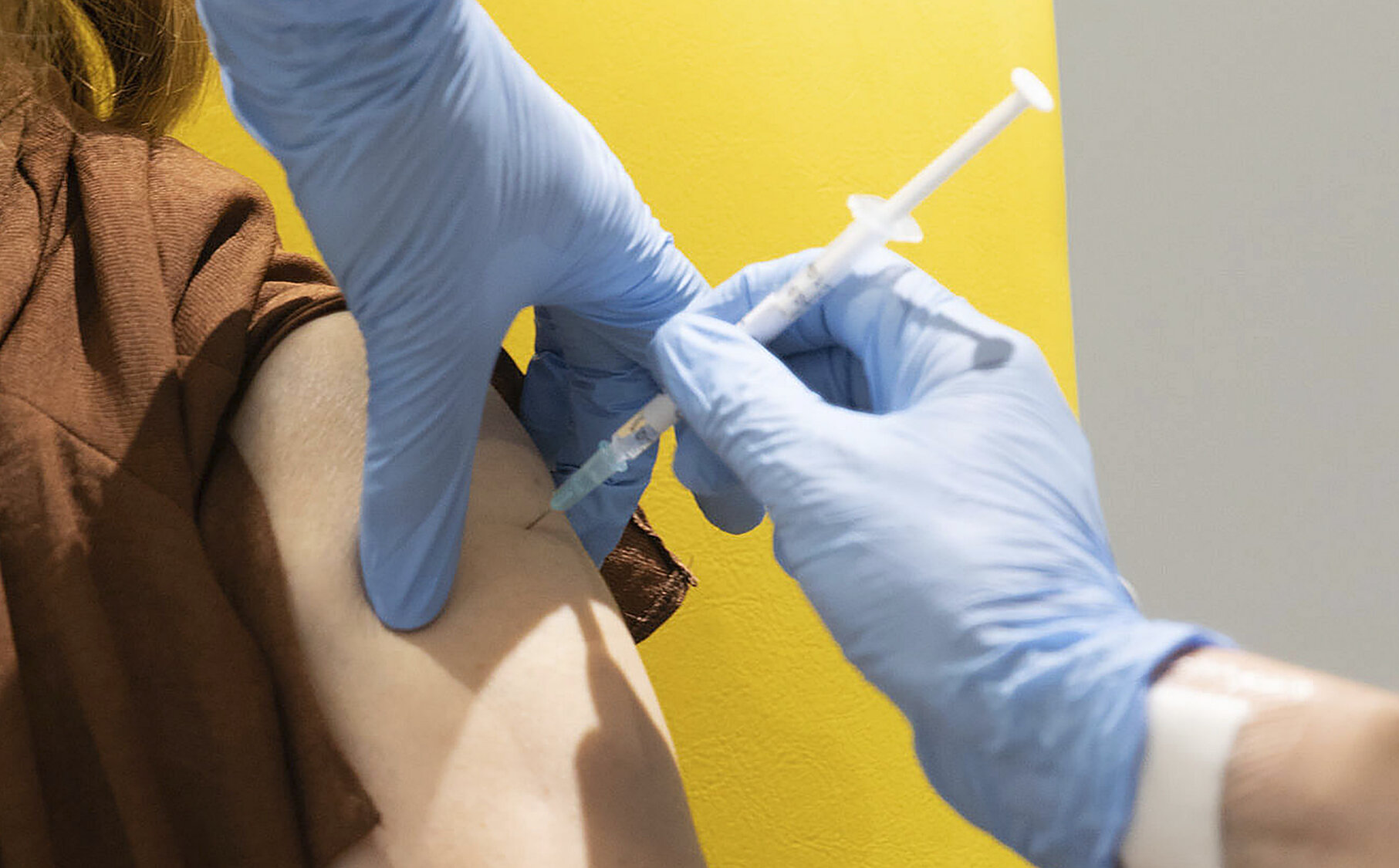
Niciodată, până la actuala criză Covid-19, vaccinurile nu au fost dezvoltate și testate într-un timp atât de scurt. Fenomenul este cu atât mai atrăgător cu cât sunt mulți candidați în cursă, iar obiectivele de vaccinare sunt globale, într-o perioadă de timp care se dorește a fi cât mai scurtă.
Cercetarea, verificarea și producerea medicamentelor de către laboratoarele farmaceutice respectă protocoale codificate. Este legitim ca mulți oameni de pe rețelele sociale să se întrebe despre consecințele vaccinării.
Pentru a obține autorizația de introducere pe piață, compania farmaceutică producătoare trebuie să prezinte autorităților sanitare rezultatele studiilor clinice de fază 3, care să dovedească eficacitatea acestora și să concluzioneze că există un echilibru favorabil între beneficii și riscuri. Cu alte cuvinte, vaccinul poate primi undă verde de la agenția pentru medicamente, chiar dacă induce efecte nedorite unor pacienți, deoarece acestea sunt considerate mai puțin dăunătoare decât beneficiul indus. Studiile de fază 3 se desfășoară pe câteva mii de persoane, adesea în mai multe țări în același timp.
„O atenție deosebită acordată potențialelor efecte adverse”
Dar monitorizarea impactului asupra sănătății nu se oprește aici. Distribuția la scară largă a vaccinului este întotdeauna însoțită de stabilirea unei faze 4 a farmacovigilenței. „Cu câteva mii de participanți selectați, faza a 3-a face posibilă identificarea celor mai frecvente efecte adverse”, explică profesorul Agnès Sommet, șeful departamentului de farmacologie al Spitalului Universitar din Toulouse. În faza 4, numărul foarte mare de persoane vaccinate în viața reală prezintă evenimente mai rare, uneori grave”.
În cazul vaccinurilor împotriva Covid-19, EMA, Agenția Europeană pentru Medicamente, este cea care centralizează dosarele de cerere; autorizația se va aplica tuturor statelor membre. Supravegherea efectelor secundare odată cu introducerea pe piață a vaccinului, reglementată de specificații stricte, este însă delegată țărilor care trebuie să analizeze și să raporteze informațiile colectate pe teritoriul lor. „Având în vedere viteza cu care au fost dezvoltate vaccinurile împotriva Covid-19, se va acorda o atenție deosebită efectelor secundare pe termen mediu și lung”, anticipează profesorul Antoine Pariente, șeful centrului de farmacovigilență din Bordeaux. Primii candidați la vaccin așteptați pe piață, cei de la Pfizer-BioNTech, Moderna și Astra-Zeneca, vor avea doar două luni de supraveghere, în medie, atunci când cer autorizația.
În mod normal, laboratoarele care comercializează vaccinuri trebuie să furnizeze Agenției Naționale pentru Siguranța Medicamentelor din Franța (ANSM) rapoarte periodice de actualizare a siguranței la fiecare șase luni, în primii ani după ce au obținut autorizația. În cazul vaccinurilor Covid, această perioadă este redusă la o lună. Aceste rapoarte vor include, printre altele, informații despre efectele secundare care au fost raportate de medici sau farmaciști sau descrise în reviste științifice, precum și date despre vânzări care vor ajuta la calcularea frecvenței efectelor secundare. EMA cere producătorilor să acorde o atenție deosebită femeilor însărcinate și vârstnicilor.
Monitorizare proactivă
În plus, studiile clinice de fază 3 nu se încheie brusc. Pot fi lansate noi teste suplimentare. La Pfizer/BioNTech, este planificată continuarea monitorizării participanților la studiile de fază 3 timp de doi ani pentru a colecta date de eficacitate și siguranță pe termen mai lung.
Sursa: Le Figaro
Dacă ti-a plăcut articolul urmărește SmartRadio pe Facebook






